Vyhliadky na produkciu systémov transfúzie krvi
Newchemistry: Aké transfúzne systémy vyrábate? JSC "Syntéza", Kurgan: Vyrábame systémy pre ...
Všetko, čo súvisí s operáciou a účinkom anestézie, sa bežne označuje ako „operačný stres“ a jej dôsledky ako „pooperačný stav“ alebo „pooperačné ochorenie“ ". Prevádzkové napätie spôsobený operačná trauma sa vyskytuje v dôsledku komplexu rôznych vplyvov: strach, vzrušenie, bolesť, vystavenie omamným látkam, trauma, rany, zdržanie sa jedenia, potreba dodržiavania pokoja na lôžku atď.
Výskyt stresového stavu uľahčujú rôzne faktory:
všeobecný stav pacienta pred operáciou a počas nej vzhľadom na charakter ochorenia;
Trauma a trvanie operácie;
Nedostatočná anestézia.
Pooperačné obdobie- obdobie od skončenia operácie po zotavenie pacienta alebo jeho presun do zdravotného postihnutia.
rozlíšiť skoré pooperačné obdobie- čas od ukončenia operácie po prepustenie pacienta z nemocnice a. \\ t
neskoré pooperačné obdobie- čas od momentu prepustenia pacienta z nemocnice do zotavenia alebo prechodu na zdravotné postihnutie.
procesy - pomer katabolizmu a anabolizmu je rozbitý.
V pooperačnom stave pacienta sa rozlišujú tri fázy(štádiá): katabolický, reverzný vývoj a anabolický.
Katabolická fázatrvá 3-7 dní. Katabolické fázy zhoršiť a rozširujú sa pripojili pooperačných komplikácií (pokračovanie krvácanie, pristúpení zápalové komplikácie, hypovolémia, zmeny vody elektrolytu a bielkovinové bilancie, ako aj poruchy v priepustnom pooperačnej bolesti nekupiruyuschiesya, chudobná, nevyvážená, parenterálnej výživa, hypoventilácia).
Keď biochemické poruchy a poruchy mikrocirkulácie primárne ovplyvňujú myokard, pečeň a obličky.
Zvýšenie rozkladu proteínov je charakteristické pre katabolickú fázu a predstavuje stratu nielen svalových proteínov, proteínov spojivového tkaniva, ale najmä straty enzýmových proteínov. Najrýchlejšie nastáva rozpad pečeňových proteínov, plazmy a gastrointestinálneho traktu a pomalšie pruhovaných svalových proteínov. Pri 24-hodinovom hladovaní sa množstvo pečeňových enzýmov znižuje o 50%. Celková strata proteínu v pooperačnom období je významná. Po resekcii žalúdka alebo gastrektómii po dobu 10 dní po operácii s nekomplikovaným priebehom a bez parenterálnej výživy stráca pacient 250-400 g proteínu, čo je 2-krát viac ako objem plazmatických proteínov a zodpovedá strate 1 700-2 000 g svalovej hmoty. Strata proteínu sa významne zvyšuje so stratou krvi, pooperačnými hnisavými komplikáciami. Strata proteínu je obzvlášť nebezpečná, ak pacient mal pred operáciou hypoproteinémiu.
Klinické prejavy katabolickej fázy pooperačného obdobia majú svoje vlastné charakteristiky.
Nervový systém, Prvý deň po operácii, kvôli reziduálnemu účinku omamných a sedatívnych látok, sú pacienti inhibovaní, ospanliví, ľahostajní k životnému prostrediu. Vo väčšine prípadov je ich správanie pokojné. Počnúc druhým dňom po operácii, keď sa zastaví pôsobenie liekov a objaví sa bolesť, môže sa objaviť úzkosť, mentálna nestabilita, ktorá môže byť vyjadrená buď v nepokojnom správaní, nepokojoch alebo naopak, depresii. Porušenie duševnej aktivity je spôsobené pridaním komplikácií, ktoré zvyšujú hypoxiu, porušovanie rovnováhy vody a elektrolytov.
Kardiovaskulárny systém, Bledosť kože, zvýšený pulz o 20–30%, mierne zvýšenie krvného tlaku. Mierny pokles objemu mŕtvice srdca je mierny.
Dýchací systém, Pacienti zaznamenali zvýšenie respirácie s poklesom hĺbky. Kapacita pľúc klesá o 30 - 50%. Plytké dýchanie môže byť spôsobené bolesťou v mieste chirurgického zákroku, vysokým postavením bránice alebo obmedzením jeho pohyblivosti po operáciách na brušných orgánoch, rozvojom parézy gastrointestinálneho traktu.
Porucha funkcie pečene a obličiek prejavuje sa zvýšením dysproteinémie, znížením syntézy enzýmov, znížením diurézy v dôsledku poklesu renálneho prietoku krvi a zvýšením obsahu aldosterónu, antidiuretického hormónu.
Fázový reverzný vývoj.Trvanie 4-6 dní. Prechod katabolickej fázy na anabolický sa nevyskytuje okamžite, ale postupne. Toto obdobie je charakterizované poklesom aktivity sympatikadrenálneho systému a katabolickými procesmi, čo dokazuje pokles vylučovania dusíka močom na 5–8 g / deň (namiesto 15–20 g / deň v katabolickej fáze). Množstvo vstrekovaného dusíka presahuje množstvo vylúčené močom. Pozitívna bilancia dusíka indikuje normalizáciu metabolizmu proteínov a zvýšenú syntézu proteínov v tele. Počas tohto obdobia sa znižuje uvoľňovanie draslíka v moči a v tele sa hromadí draslík, ktorý sa podieľa na syntéze proteínov a glykogénu. Obnovuje sa rovnováha vody a elektrolytu. V neurohumorálnom systéme prevláda vplyv parasympatického systému, zvyšuje sa hladina somatotropného hormónu, inzulínu, androgénov.
V prechodnej fáze pokračuje zvýšená spotreba energie a plastových materiálov (bielkovín, tukov, sacharidov), aj keď v menšej miere, ktorá sa postupne znižuje, a aktívna syntéza proteínov, glykogénu a potom tukov, ktoré sa zvyšujú s poklesom katabolickej intenzity. procesy. Konečná prevaha anabolických procesov nad katabolickým javom indikuje prechod pooperačného obdobia v anabolickej fáze. Fáza reverzného vývoja nastáva 3 - 7 dní po operácii pre nekomplikované pooperačné obdobie. Známky konca katabolickej fázy a nástup reverznej vývojovej fázy sú zmiznutie bolesti, normalizácia telesnej teploty, vzhľad apetítu. Pacienti sa stávajú aktívnymi, koža sa stáva normálnou farbou, dýchanie sa stáva hlbokým, počet dýchacích pohybov sa znižuje. Srdcová frekvencia sa blíži počiatočnej predoperačnej úrovni. Obnovuje sa aktivita gastrointestinálneho traktu: objavuje sa peristaltický intestinálny hluk, plyny sa začínajú odchyľovať.
Anabolická fáza.Vyznačuje sa zvýšenou syntézou proteínu, glykogénu, tukov spotrebovaných počas operácie a katabolickej fázy pooperačného obdobia.
Povaha neuroendokrinnej reakcie sa prejavuje aktiváciou parasympatického autonómneho nervového systému a zvýšením aktivity anabolických hormónov. Syntéza proteínov je stimulovaná somatotropným hormónom hypofýzy a androgénov, ktorých aktivita v anabolickej fáze je významne zvýšená. Rastový hormón zvyšuje transport aminokyselín z medzibunkových priestorov do bunky. Syntéza proteínov v pečeni, obličkách, myokarde je aktívne ovplyvnená androgénmi. Určité hormonálne procesy vedú k zvýšeniu množstva proteínov v krvi, orgánoch, ako aj v oblasti rany, čím sa zaisťujú reparatívne procesy, rast a vývoj spojivového tkaniva.
V anabolickej fáze pooperačného obdobia sa obnovujú zásoby glykogénu.
Klinické príznaky charakterizujú anabolickú fázu. ako obdobie zotavenia, obnovenie zhoršených funkcií kardiovaskulárnych, respiračných, vylučovacích systémov, zažívacích orgánov, nervového systému. V tejto fáze sa zdravotný stav pacienta zlepšuje, chuť do jedla sa zvyšuje, srdcová frekvencia a krvný tlak sú normalizované, aktivita gastrointestinálneho traktu je obnovená: prechod potravy, proces vstrebávania v čreve, objavenie sa samostatného kresla.
Trvanie anabolickej fázy - 2-5 týždňov. Jeho trvanie závisí od závažnosti operácie, počiatočného stavu pacienta a závažnosti a trvania katabolickej fázy. Táto fáza pooperačného obdobia je ukončená pridaním telesnej hmotnosti, ku ktorej dochádza v priebehu 3-4 týždňov a pokračuje až do úplného zotavenia, ktoré niekedy trvá niekoľko mesiacov. V priebehu 3 - 6 mesiacov sa nakoniec ukončia procesy reparatívnej regenerácie - dozrievanie spojivového tkaniva, tvorba jaziev.
Po operácii sa pacienti prijímajú na jednotku intenzívnej starostlivosti alebo do oddelenia, ktoré sú špeciálne organizované na monitorovanie pacientov, vykonávanie intenzívnej starostlivosti a v prípade potreby poskytovanie pohotovostnej starostlivosti. Na monitorovanie stavu pacienta v oddeleniach sú zariadenia, ktoré umožňujú neustále zaznamenávať frekvenciu pulzov, rytmus, EKG, EEG. Expresné laboratórium vám umožňuje sledovať hladinu hemoglobínu, hematokritu, elektrolytov, krvných proteínov, BCC, acidobázického stavu. Jednotka intenzívnej starostlivosti má všetko, čo potrebujete na poskytovanie pohotovostnej starostlivosti: súbor liekov a transfúznych médií, zariadenie na mechanickú ventiláciu, sterilné súpravy na venesekciu a tracheostómiu, zariadenie na defibriláciu srdca, sterilné katétre, sondy vybavené toaletným stolíkom.
Dôkladné vyšetrenie pacienta sa vykonáva pomocou všeobecných metód klinického vyšetrenia: vyšetrenie, palpácia, perkusia, auskultizácia a v prípade potreby inštrumentálne vyšetrenie (elektrokardiografia, röntgenové žiarenie, elektroencefalografia atď.). Pacientov psychický stav (vedomie, správanie - vzrušenie, depresia, bludy, halucinácie), jeho koža (bledosť, cyanóza, žltačka, suchosť, potenie) sa neustále monitoruje.
V štúdii kardiovaskulárne systémy určujú tepovú frekvenciu, plnenie, rytmus, úroveň arteriálneho av prípade potreby centrálneho venózneho tlaku, charakter zvukov srdca, prítomnosť hluku. V štúdii dýchacích orgánov odhadnúť frekvenciu, hĺbku, rytmus dýchania, vykonať perkusie a auskultizáciu pľúc.
V štúdii tráviace orgány určiť stav jazyka (suchosť, prítomnosť nájazdov), brucha (nadúvanie, účasť na dýchaní, prítomnosť príznakov peritoneálneho podráždenia: napätie svalov brušnej steny, Shchetkinov príznak - Blumberg, prítomnosť peristaltického intestinálneho hluku), palpácia pečene. Od pacienta dostávať informácie o vypúšťaní plynu, prítomnosť stoličky.
študovať močového systému zahŕňa stanovenie dennej diurézy, rýchlosť močenia permanentného močového katétra.
Analyzujú sa aj laboratórne údaje (hemoglobín, hematokrit, stav kyslej bázy, BCC, krvné elektrolyty). Zmeny laboratórnych parametrov spolu s klinickými údajmi nám umožňujú správne určiť zloženie a objem transfúznej terapie, predpisovanie liekov.
Vyšetrenie pacienta sa vykonáva opakovane, aby sa porovnali údaje a včas sa zistilo možné zhoršenie jeho stavu, identifikovali sa včasné príznaky možných komplikácií a čo najskôr sa začala liečba.
Údaje z inšpekcií a špeciálnych štúdií sa vkladajú do špeciálnej karty na monitorovanie pacienta na jednotke intenzívnej starostlivosti a sú zaznamenané v histórii prípadu vo forme záznamov z denníka.
Pri monitorovaní by sa mal pacient zamerať na kritické ukazovatele výkonnosti orgánov a systémov ktoré by mali slúžiť ako základ pre zistenie príčiny zhoršenia stavu pacienta a poskytovania pohotovostnej starostlivosti: \\ t
1) stav kardiovaskulárneho systému: srdcová frekvencia viac ako 120 úderov / min; pokles systolického krvného tlaku na 80 mm Hg. Art. a pod a nárast na 200 mm Hg. v.; porucha srdcového rytmu; pokles centrálneho venózneho tlaku pod 50 mm vody. Art. a zvýšiť ju na viac ako 11 mm vody. v.;
2) stav dýchacieho systému: počet dychov viac ako 28 za minútu; výrazné skrátenie bicieho zvuku, matný zvuk nad pľúcami počas perkusie hrudníka; nedostatok dýchacieho hluku v zóne otupenia;
3) stav kože a viditeľných slizníc: ťažká bledosť; akrozianoz; studený lepkavý pot;
4) stav vylučovacieho systému: zníženie močenia (množstvo moču je menšie ako 10 ml / h); anúria;
5) stav orgánov gastrointestinálneho traktu: ostré napätie svalov prednej brušnej steny; čierne výkaly, krv vo výkaloch; prudko pozitívny symptóm Shchetkina - Blumberg; výrazná abdominálna distenzia, neprostup plynu, nedostatok peristaltického intestinálneho hluku viac ako 3 dni;
6) stav centrálneho nervového systému: strata vedomia; halucinácie, halucinácie; motorové, rečové vzrušenie; inhibovaný stav
7) stav rany: hojné namáčanie krvných obväzov; divergencia okrajov rany, vznik brušných orgánov v rane (eventácia); nadmerné zmáčanie obväzu hnisom, črevným obsahom.
Liečbu.Kompenzujte metabolické poruchy, obnovte poškodené funkcie orgánov, normalizujte redox procesy v tkanivách - dodávku kyslíka, vylučovanie oxidovaných metabolických produktov, oxid uhličitý a obnovte zvýšené náklady na energiu.
Dôležitou metódou udržiavania a zlepšovania metabolizmu proteínov a elektrolytov je parenterálna a, ak je to možné, enterálna výživa pacienta. Mali by ste uprednostniť zavedenie tekutín a živín prirodzeným spôsobom a používať ich čo najskôr.
Hlavné body intenzívnej starostlivosti v pooperačnom období
1. Boj proti bolesti s použitím liekov proti bolesti, elektroanalgézie, epidurálnej anestézie atď.
2. Obnova kardiovaskulárnej aktivity, eliminácia mikrocirkulačných porúch (kardiovaskulárne látky, reopolyglukín).
3. Prevencia a liečba respiračného zlyhania (kyslíková terapia, dychové cvičenia, riadené vetranie).
4. Detoxikačná terapia.
5. Korekcia metabolických porúch (rovnováha vody a elektrolytov, acidobázický stav, syntéza proteínov).
6. Vyvážená parenterálna výživa.
7. Obnovenie funkcie vylučovacieho systému.
8. Obnovenie funkcie orgánov, ktorých aktivita je zhoršená v dôsledku chirurgickej expozície (črevná paréza počas operácií na brušných orgánoch, hypoventilácia, atelektáza počas pľúcnych operácií atď.).
Úspechy modernej anestéziológie umožňujú zabezpečiť stabilný stav hlavných funkcií tela počas operácie. Po ukončení chirurgického zákroku a odchode pacienta zo stavu anestézie však puerperálny organizmus vstúpi do stavu, v ktorom chýbajú ochranné vlastnosti celkovej anestézie a začnú pôsobiť bolesti, toxické a emocionálne faktory. Pre mnoho pacientov je preto pooperačné obdobie podstatne náročnejšie ako samotná operácia.
Nepostrádateľnou podmienkou na zabezpečenie normálnej pooperačnej rehabilitácie je znalosť zmien, ku ktorým dochádza v tele pacienta po operácii, vlastníctvo metód na prevenciu a liečbu pooperačných komplikácií. V skorom pooperačnom období dochádza k reziduálnemu účinku svalových relaxancií, postnarkotickej depresii, silnej bolesti, až do vzniku šoku, vzniku akútnych kardiovaskulárnych a respiračných, hepatálnych, renálnych zlyhaní, metabolických porúch, rovnováhe vody a elektrolytov, stavu acidobázickej rovnováhy a hemostáze. , Preto je jasné, že objem a kvalita intenzívnej starostlivosti v ranom období rehabilitácie závisí od vyššie uvedených bodov.
Intenzívna pooperačná terapia je svojím obsahom kombináciou preventívnych a terapeutických opatrení, ktoré zabezpečujú udržanie alebo dokonca dočasnú náhradu životne dôležitých funkcií v prípade alebo len v prípade hrozby kritického poškodenia. Úlohou intenzívnej starostlivosti je v konečnom dôsledku prevencia pooperačných komplikácií, udržanie a obnovenie stálosti vnútorného prostredia tela, ktorého zmeny sú spôsobené operáciou a anestéziou.
Po úplnom prebudení z anestézie, pretrvávajúcom dýchaní, normalizácii hemodynamiky, pri absencii komplikácií počas chirurgického zákroku a anestézii sa puerperál prenesie na oddelenie. V prvých hodinách po operácii je potrebné sledovať sekréty z genitálneho traktu, veľkosť maternice, pulz a krvný tlak ženy, ako aj včasné vyprázdnenie močového mechúra. Okamžite predpíšte chlad a závažnosť (ľadový obklad) na bruchu počas 2 hodín Infúzia 5 U oxytocínu, 5 mg enaprostu v 5% roztoku glukózy alebo izotonický roztok chloridu sodného je indikovaná podľa indikácií (zhoršená kontraktilita maternice, konzervatívna myomektómia, atď.). ).
Počas prvej hodiny po operácii sa každých 15 minút kontroluje srdcová frekvencia, krvný tlak, rýchlosť dýchania a stav elektrokardiogramu monitorom na nočnom stolíku. Lekár alebo jeho asistent vyšetrí pacienta 20 minút po operácii, potom po 30 minútach, po 1 hodine a po niekoľkých hodinách, aby sa ubezpečil, že stav puerperu je stabilný a nie je krvácanie.
Nevoľnosť, nutkanie na zvracanie a vracanie sú najčastejšie pooperačné komplikácie, ktoré sa môžu vyskytnúť po celkovej, regionálnej a lokálnej anestézii. Nevoľnosť je definovaná ako subjektívne nepríjemný pocit spojený s blížiacim sa nutkaním zvracať. Typicky sa tento pocit vyskytuje v zadnej časti hrdla a epigastrickej oblasti a je sprevádzaný stratou tonusu žalúdka, redukciou dvanástnika a vyprázdňovaním črevného obsahu do žalúdka. Nutkanie na zvracanie je definované ako nevyhnutné, kŕčovité, rytmické kontrakcie dýchacích svalov, vrátane bránice, svalov hrudníka a brušnej steny bez vypudenia obsahu žalúdka. Zvracanie je nútené vypudenie obsahu žalúdka ústami, ktoré je dôsledkom silného kontinuálneho sťahovania brušných svalov, znižovania diafragmy a otvárania srdcovej drene žalúdka. Výskyt zvracania je ovplyvnený nasledujúcimi faktormi: vek pacienta, obezita, úzkosť, paréza žalúdka, chirurgické zákroky, ich objem, typ anestézie.
Na prevenciu a liečbu pooperačného zvracania môžete použiť: fenotiazíny (2,5% roztok aminazínu - 1 - 2 ml, 2,5% roztok diprazínu - 2 ml), deriváty butyrofenónu (haloperidol 1-2 ml - 0,5% roztok, talomonal - 2 ml, atď.), Antihistaminiká (difenhydramín, suprastín, atď.), Benzamidy (dogmatil, eglonid 2 ml 5% roztoku), anticholinergiká (atropín, platyfillín atď.).
Frekvencia pooperačného zvracania je 20-30%, čo je výrazne nižšie ako frekvencia (75-80%), zaznamenaná v "ére éterovej anestézie".
Nevoľnosť a zvracanie môžu viesť k dehydratácii a elektrolytovej nerovnováhe, najmä pri ambulantnej chirurgii. Opakované nutkanie na zvracanie alebo zvracanie môže viesť k napätiu línie stehu, venóznej hypertenzii, zvýšenému krvácaniu. Okrem toho sa zvyšuje riziko aspirácie zvracania, keď sú respiračné reflexy potlačené v dôsledku reziduálneho účinku použitia anestetík alebo analgetík. Prvým dôležitým faktorom, ktorý treba v pooperačnom období venovať pozornosť, je výskyt hypovolémie. Hypovolémia je redukcia bcc bez ohľadu na etiológiu (preeklampsia, strata krvi, poruchy kardiovaskulárneho systému, atď.). Klinické a fyziologické účinky hypovolémie môžu byť znázornené nasledovne (schéma 5).
Detekcia hypovolémie sa vykonáva podľa vyššie uvedených klinických prejavov, objektívnymi kritériami sú veľkosť BCC a CVP. Podľa mnohých autorov sú normálne indexy CVP v rozmedzí 0,2–1,2 kPA (20–120 mm vody. Čl.). Pre resuscitátory nie je najdôležitejšia absolútna hodnota CVP ako jeho dynamika v závislosti od stavu pacienta a vykonanej terapie.
Hypovolémia vždy vedie k zhoršenej mikrocirkulácii, ktorej kritériom je porucha diurézy menej ako 0,5 ml / min, teplotný gradient medzi kožou a konečníkom viac ako 4 °, prítomnosť metabolickej acidózy, pokles indexu arteriovenózneho kyslíka.
Pokles krvného tlaku so zvýšením srdcovej frekvencie, vláknitého pulzu a nízkou hodnotou hematokritu indikuje prítomnosť krvácania. V takýchto prípadoch by sa mala naliehavo riešiť otázka ďalšej spoločnej taktiky.
Je potrebné mať na pamäti, že bledosť kože a slizníc, rýchly pulz, nižší krvný tlak môže indikovať hypovolémiu. Pochybnosť v správnej diagnóze nezostane, ak zmeráte centrálny venózny tlak. Nízke sadzby potvrdia jeho hypovolemický stav. Nízky krvný tlak na pozadí vysokých venóznych, dobrých vyplnení žíl končatín, tachykardie a zodpovedajúce zmeny v elektrokardiograme zároveň indikujú, že pacient má srdcovú slabosť.
V pôrodníckej praxi v neprítomnosti ochorení kardiovaskulárneho systému a komplikovaného priebehu tehotenstva (gestaza) je príčinou nestabilnej hemodynamiky najčastejšie hypovolémia v dôsledku nenaplnenej straty krvi. Adekvátne a včasné doplnenie krvnej straty je jednou z hlavných podmienok stabilizácie hemodynamiky a normálneho priebehu pooperačného obdobia.
Spolu s nahradením straty krvi je mimoriadne dôležité korigovať stav kyseliny a bázy, pretože je ťažké obnoviť a stabilizovať hemodynamiku v podmienkach acidózy. Zavedenie vazokonstrikčných liečiv na zvýšenie krvného tlaku je nežiaduce, pretože vaskulárny spazmus vyplývajúci z tohto zhoršuje tok krvi do tkanív a orgánov a vytvára len ilúziu pohody v dôsledku normálneho alebo vysokého krvného tlaku. Preto je potrebné monitorovať stav prietoku krvi v periférnom tkanive, a nie len úroveň krvného tlaku. Indikáciou zavedenia vazokonstrikčných liečiv je vaskulárny kolaps.
V prípade srdcovej slabosti je potrebná komplexná liečba: intravenózne podávanie srdcových glykozidov (strofantín, korglikon), hormonálnych liekov (hydrokortizón, prednizolón), dopamínu, izadrínu, vitamínov s glukózou atď.
Výskyt rôznych arytmií u ľudí so zdravým srdcom bude v prvom rade indikovať poruchu normálneho obsahu kyslíka a oxidu uhličitého v krvi, zvyčajne v dôsledku nedostatočného vetrania pľúc (samostatné alebo umelé). Príčinou arytmií môže byť aj hyperadrenalínia, metabolická acidóza, nerovnováha elektrolytov v krvi a srdcovom svale, rôzne mechanické faktory, ktoré dráždia (drenáže, tampóny, intubačná trubica atď.).
Výskyt arytmií vyžaduje okamžitý a aktívny zásah, pretože nielenže zhoršuje hemodynamiku, ale môže tiež spôsobiť ventrikulárnu fibriláciu. Osobitnú pozornosť treba venovať predčasným komorám. Účinné pri arytmiách lidokaín a izoptín, podávané intravenózne v dávkach 60-80, respektíve 5-10 mg.
V skorom post-anestetickom období je možná reziduálna depresia a jej účinok na funkčný stav centrálneho nervového systému, kortikálnych štruktúr a neurovegetatívnych štruktúr. Za týchto podmienok majú pacienti zníženú odolnosť voči bolesti, čo vedie k vyčerpaniu vyšších funkcií centrálneho nervového systému, k ochranným a adaptívnym reakciám, k ešte väčšiemu zníženiu prahu vnímania bolesti.
Pri nekomplikovanom pooperačnom období je bolesť najčastejšou a niekedy jedinou príčinou emocionálneho vyčerpania pacientov, porúch močenia, paretického stavu žalúdka a čriev. V dôsledku toho, v bezprostrednom pooperačnom období, anestéziológ čelí úlohe zmierniť faktor bolesti, predchádzať vyčerpaniu centrálneho nervového systému, zvyšovať odolnosť tela, znižovať negatívne účinky spojené s operáciou a anestéziou.
Z farmakologických liečiv na pooperačnú analgéziu, narkotiká a narkotiká analgetiká sa v súčasnosti používa kombinácia neuroleptík, antispazmodík, hypnotík, sedatív, ako aj mnohých liekov všeobecného narkotického účinku.
V prvých 2-3 hodinách po chirurgickom zákroku sa odporúča použiť narkotické analgetiká, ktorých hlavnými predstaviteľmi sú deriváty kyseliny salicylovej (salicyláty) - salicylát sodný, kyselina acetylsalicylová, salicylamid atď. pyrazolónové deriváty - antipyrín, analgín; deriváty para-aminofenolu (alebo anilínu) - fenacetín, paracetamol; antagonisty - agonisty opiátového receptora (moradol, tramal, pentazocín atď.).
Napriek tomu, že narkotické analgetiká sú významne menej účinné ako lieky podobné morfínu, pokiaľ ide o ich účinok, sú zbavené mnohých vedľajších účinkov na telo pacienta: neexistuje žiadny inhibičný účinok na respiračné a antitusické centrá a absencia eufórie a psychickej a fyzickej závislosti.
Na dosiahnutie výraznejšej a pretrvávajúcej anestézie sa používajú narkotické analgetiká. Patrí medzi ne morfín, promedol, dipidolor, omnopon, fentanyl a ďalšie, ktoré by sa nemali používať skôr ako 2-3 hodiny po operácii, aby sa zabránilo zvýšeniu depresie lieku a reziduálnych účinkov anestézie. Používať použitie narkotických analgetík by malo byť v prvých 2-3 dňoch po operácii, čo výrazne znižuje počet injekcií s každým nasledujúcim dňom.
Antihistaminiká, sedatíva, antispasmodiká, hypnotiká a iné liečivá sa používajú spolu s nimi na zvýšenie analgetických a hypnotických účinkov analgetík a iných analgetík. V niektorých situáciách sa na účely pooperačnej analgézie používajú neuroleptická algézia, elektroanalgézia a epidurálna anestézia.
Osobitná pozornosť v pooperačnom období vyžaduje jeden z dôležitých systémov puerperálneho tela - respiračný.
Stav pľúcnej ventilácie a výmeny plynov v nasledujúcich hodinách po operácii môže byť spôsobený charakteristikami anestézie, povahou chirurgického zákroku, hlavným patologickým procesom a prítomnosťou sprievodných ochorení. Nasledujúci deň po operácii je príčinou respiračného zlyhania pľúcne komplikácie, ktoré sa vyvíjajú na pozadí hypovolemických, mikrocirkulačných, zápalových a metabolických porúch.
Respiračné zlyhanie centrálnej genézy nastáva po operácii z dôvodu narkotickej depresie respiračného centra pod vplyvom anestetík a narkotických analgetík, ktoré sa používali počas operácie, kde dochádza k hypoxickému cerebrálnemu edému v šestonedeliach s eklampsiou, obehovými a metabolickými poruchami.
Jeho prevencia spočíva vo výbere optimálnej metódy a celkovej dávky narkotík a sedatív s prihliadnutím na všeobecný stav puerperálne ženy, charakter patofyziologických zmien, vykonávanie primeranej umelej ventilácie pľúc počas operácie, stanovenie spoľahlivých kritérií pre extubáciu (príznaky úplného obnovenia dýchania, vedomia, svalového tonusu, stabilnej hemodynamiky atď.). Princíp intenzívnej terapie akútnych respiračných porúch centrálnej genézy spočíva v vykonaní umelej ventilácie pľúc (jej metódy a varianty sú určené povahou a závažnosťou respiračných porúch a podmienkami ich výskytu).
V prípade respiračného zlyhania spôsobeného reziduálnou kurarizáciou alebo rekurarizáciou vedie táto porucha v neprítomnosti adekvátneho lekárskeho dohľadu k zhoršenej výmene plynov a zástave srdca. Prevencia tohto typu porúch spočíva v optimálnom výbere typu, dávky a spôsobu použitia svalových relaxancií, adekvátnom zhodnotení stupňa obnovy svalového tonusu pred extubáciou, včasnej diagnostike porúch homeostázy a korekčnej terapii metabolických porúch, dynamickom sledovaní ich účinku alebo predĺženom umelom dýchaní až do úplného zotavenia. spontánne dýchanie.
Princípy intenzívnej terapie spočívajú v udržiavaní výmeny plynov umelým vetraním pľúc na pozadí korekcie hypoproteinémie, hypokalémie, anémie, metabolickej acidózy, ktorá je často hlavným faktorom tohto typu respiračného zlyhania.
Respiračné zlyhanie môže byť spojené s pooperačnými pľúcnymi komplikáciami (atelektáza, pneumónia). Príčiny atelektázy sú neuro-reflexné faktory spôsobené zhoršením pľúcneho prietoku krvi, bronchiálnou obštrukciou hlienom, kompresiou pľúc zvonka vzduchom a výpotkom. Bez ohľadu na príčinu existuje vo všetkých prípadoch prvok obštrukcie dýchacích ciest.
Prevencia pľúcnej atelektázy sa skladá zo série aktivít, z ktorých najdôležitejšie sú správna voľba metóda celkovej anestézie s výnimkou liekov a anestetík, ktoré zhoršujú drenážnu funkciu epitelu ciliárneho bronchiálneho aparátu, starostlivú a starostlivú rehabilitáciu tracheobronchiálneho stromu, použitie zmesi narkotík s obsahom plynu najviac 40% kyslíka, vykonávanie umelej ventilácie pľúc s optimálnymi parametrami objemu a tlaku, úplná anestézia s výnimkou subkutánneho podávania analgetík oslabeným pacientom, včasná aktivácia pacienta v posteli, posturálna drenáž a vibrácie hrudná masáž, aerosólová terapia, použitie bronchodilatátorov a kortikosteroidov, dynamické röntgenové vyšetrenie a laboratórne monitorovanie. V prípade potreby preneste pacienta na umelú ventiláciu pľúc.
V pooperačnom období sa častejšie vyvíja atelektická, aspiračná a hypostatická forma pneumónie. Atelektická pneumónia sa prejavuje príznakmi atelektázy a zápalu, ktorý je s ňou spojený, aspirácia je charakterizovaná príznakmi výraznej bronchitídy, bronchiolospazmu, bolesti za hrudnou kosťou, kašľa atď. Pre hypostatickú pneumóniu sú neskoršie obdobia vývoja charakterizované celkovým vážnym stavom pacienta. Je výsledkom fyzickej nečinnosti, hypoventilácie, porúch obehu v malom kruhu, zlyhania srdca a zníženia imunologickej reaktivity tela.
Prevencia pneumónie je tiež zložená z viacerých aktivít, z ktorých je veľmi dôležitá rehabilitácia ústnej dutiny, hltanu, horných dýchacích ciest, adekvátnej celkovej anestézie s obmedzenými farmakologickými látkami, respiračnej depresie a funkcie epitelu rias. Dôležitá je prevencia zvracania, regurgitácie, aspirácie, starostlivej intubácie, atraumatickej rehabilitácie tracheobronchiálneho stromu počas operácie, doplňovania prevádzkovej straty krvi, eliminácie hypovolémie, adekvátnej umelej ventilácie počas anestézie, včasnej aktivácie pacienta a zvýšenej imunologickej rezistencie.
Intenzívna starostlivosť pneumónia zahŕňa dychové cvičenia, kyslíkovú terapiu, zavedenie nástrojov, ktoré zlepšujú dýchacie funkcie priedušiek a riedenie spúta, použitie antihistaminík, bronchodilatátorov, kortikosteroidov, aerosólovú terapiu, stimuláciu kašľa, infúznu terapiu zameranú na udržanie rovnováhy tekutín, použitie srdcových glykozidov, vitamínov, karbocytoxylátov ; s progresívnym zlyhaním dýchania - prechod na umelú ventiláciu pľúc.
Po cisárskom reze sa hypovolémia vyskytuje vždy a poruchy mikrocirkulácie sa vyvíjajú v dôsledku veľkej straty tekutín na pozadí. Na pozadí hypovolémie nie je profylaktické podávanie antibiotík dostatočne účinné.
Vzhľadom na tieto údaje v pooperačnom období je potrebné venovať osobitnú pozornosť infúznej transfúznej terapii, ktorej cieľom je: eliminovať deficit globulárneho objemu (krv, erytromas), obnoviť deficit objemu plazmy (koloidy a kryštaloidy), korigovať poruchy metabolizmu vody a elektrolytov a metabolizmus proteínov, zlepšenie reologických vlastností krvi a mikrocirkulácie.
Prvý deň po operácii bez komplikovaného prietoku sa nemá vstreknúť viac ako 1,5-2 litrov tekutiny, z toho 800 ml koloidné roztoky (polyglyukín, reoprgliglyukín, plazma, albumín), zvyšok objemu tvoria kryštaloidné roztoky (laktosol, 10% roztok glukózy, obsahujúce najmenej 4 - 6 g draslíka). Podľa indikácií (masívna strata krvi, hypertermia, dýchavičnosť, črevná paréza atď.) Objem infúznej terapie by sa mali zvýšiť. V poslednej dobe sa v pôrodníckej praxi stále častejšie objavujú zástupcovia novej triedy náhrad plazmy, prípravkov hydroxyetylškrobu (Infukol HES 6% a HAES ster 6%), ktoré majú minimálne vedľajšie účinky, spolu s ich prirodzenými hemodynamickými a reologickými vlastnosťami, ktoré by sa mali v tomto štádiu zvážiť. ako dokonalý infúzne médium na korekciu hypovolémie, hemorheologických porúch a koloidno-osmotickej insuficiencie.
Dôležitá je aj udržiavanie rovnováhy tekutín a elektrolytov. Je známe, že denná potreba vody pre dospelého je 30 až 35 ml / kg telesnej hmotnosti (2500 ml). Je zrejmé, že rovnaké množstvo sa vylučuje z tela: 1300-100 ml močom, 300-400 ml potných žliaz, 400-600 ml vydychovaného vzduchu a asi 100 ml výkalmi.
Spolu s kvapalinou sa uvoľňujú aj elektrolyty, ktorých dokončenie je tiež nevyhnutné. V priebehu dňa sa z tela vylučuje 120 mmol sodíka a 90 mmol draslíka. Normálne je rovnováha vody a elektrolytov v stave dynamickej rovnováhy. Tehotenstvo a cisársky rez porušujú.
V pooperačnom období by sa na prevenciu závažných komplikácií mali intravenózne podávať tekutiny a elektrolyty s použitím veľkých ciev, aby sa zabránilo výskytu flebitídy. Izotonický roztok chloridu sodného, 5% roztoku glukózy a 3% roztoku chloridu draselného sa zvyčajne používa na kompenzáciu straty tekutiny a elektrolytov. Pri adekvátnej diuréze sa po operácii uvoľní 3-4 g draslíka denne. Toto množstvo sa má podávať v 500 ml 5% roztoku glukózo-inzulínovej zmesi pod kontrolou hladiny draslíka v krvi. So zvyšujúcou sa telesnou teplotou sa strata tekutiny na deň zvyšuje na 500 ml na stupeň. Pri posudzovaní vodnej bilancie je potrebné brať do úvahy subjektívny zdravotný stav pacienta, stav kože, diurézu, hematokrit a celkový obsah proteínov v krvnom sére. V puerperách s ťažkou preeklampsiou a chorobami kardiovaskulárneho systému by sa zavedenie tekutiny malo vykonávať s veľkou opatrnosťou pod neustálou kontrolou centrálneho venózneho tlaku. Ak napriek zavedeniu tekutiny centrálny venózny tlak klesne a hodnota hematokritu sa zvýši, plazma alebo sérový albumín, roztok etoxylovaného škrobu by sa mal podať infúziou, aby sa zvýšil onkotický tlak a tým sa udržala tekutina v krvných cievach. Treba dbať na to, aby sa zabezpečili dodatočné straty tekutín v dôsledku zvracania alebo hnačky a aby sa okamžite kompenzovali.
Požadovaný objem tekutiny by mal zahŕňať roztoky na parenterálnu výživu. V skorom pooperačnom období sa vykonáva, keď je orálna výživa nemožná v dôsledku dysfunkcie žalúdka a čriev (rany, resekcia čriev atď.), Aby sa znížilo rozpad proteínov v prvej, katabolickej fáze.
Pri parenterálnej, ako aj enterálnej výžive je potrebné vyhovieť potrebám tela pre energiu, aminokyseliny, esenciálne mastné kyseliny, minerály a vitamíny. Hlavným zdrojom energie sú sacharidy a tuky, zdrojom aminokyselín sú rôzne proteínové prípravky, zmesi aminokyselín.
Je potrebné pripomenúť, že pri vykonávaní parenterálnej výživy sa môže vyskytnúť hyperhydratácia, ktorá je nežiaduca, najmä u žien s ochoreniami kardiovaskulárneho systému a obličiek, ako aj pri ťažkých formách preeklampsie.
V tejto súvislosti je potrebné okrem zmesí aminokyselín a hydrolyzátov proteínov aplikovať vysoko koncentrované (10-20%) roztoky glukózy a tukové emulzie (intralipid, lipofundin), ktorých malé množstvá nesú veľké množstvo energie. Zavedenie glukózy musí byť sprevádzané zavedením inzulínu (v množstve 1 U inzulínu na 3-4 g suchej glukózy).
Strata 15 až 25% telesnej hmotnosti je spojená s hrozbou poklesu obranných mechanizmov a zlého hojenia rán a vyžaduje, aby potreba všetkých živín pre telo bola povinná a úplne splnená.
Denná potreba živín, poskytujúca 8792 kJ (2000 kcal) energie, je teda 0,7-1 g / kg telesnej hmotnosti (70 g) aminokyselín, 225 g sacharidov a asi 100 g tuku. To sa dosiahne napríklad zavedením 1 1 aminokyselín, 500 ml intralipidu a 1 1 10% roztoku glukózy. Ak vezmeme do úvahy tekutinu zavedenú intraoperačne a potrebné nápravné riešenia, je zrejmé, že nie je možné uskutočniť úplnú parenterálnu výživu prvý deň po operácii. Je vhodnejšie obmedziť na polovicu vypočítaných dávok roztokov na parenterálnu výživu. V nasledujúcich dňoch sa má program infúznej terapie zostaviť s povinným údajom a zahrnutím potrebného objemu a kvality parenterálnej výživy.
Najneskôr 18-24 hodín po operácii je potrebné začať stimuláciu funkcie žalúdka a čriev. Najjednoduchší spôsob stimulácie je alimentárne. Musíte začať s požitím 50 ml teplej vodyPo 40-60 minútach sa pacientovi umožní vypiť ďalších 100 ml vody. Uistite sa, že evakuácia tekutiny zo žalúdka do čreva nastane bez omeškania, o čom svedčí neprítomnosť nepríjemných pocitov v žalúdku, nevoľnosť, vracanie, dávkovanie vody v malých porciách. Na druhý deň je predpísaná tekutá strava (kefír, čaj, vývar) na 3. - polotekutej strave (slizové polievky, varené vajce, tvaroh, tekutá kaša, kyslé mlieko), 5-8 dní s nekomplikovaným pooperačným zákrokom V tomto období sa pacienti presunú na všeobecnú stravu.
V nekomplikovanom pooperačnom období sa zvyčajne aktivuje črevná motilita na druhý deň po operácii. Auscultationally počúva dobrú peristaltiku, plyny unikajú samy od seba, na 3. deň dochádza k spontánnej defekácii. Avšak v mnohých puerperách sa peristaltika čriev znižuje v prvý deň pooperačného obdobia a vyvíja sa jej paréza. Klinicky sa to prejavuje abdominálnou distenziou, retenciou plynu. Rýchle odstránenie parézy a paralýzy čriev je jedným z naliehavých bodov pri liečení septických komplikácií, pretože paréza vedie k zhoršeniu už existujúcej hypoxie črevnej steny v dôsledku vývoja ischémie. Včasné obnovenie peristaltiky prispieva okrem toho k zvýšeniu priechodnosti portálneho krvného obehu a tým k zlepšeniu prívodu kyslíka a funkcie pečene.
Je možné zabrániť vzniku črevnej parézy. To sa dosahuje aktívnym riadením pooperačného obdobia (dychové cvičenia, aktívne správanie v posteli, skoré stúpanie, vykonávanie komplexu všeobecných terapeutických cvičení).
Obnovenie svalového tonusu črevnej steny sa dosahuje dekompresiou gastrointestinálneho traktu (drenáž žalúdka a počiatočná časť tenkého čreva sondou, nahradenie črevných plynov kyslíkom, opláchnutie žalúdka ľahkou premývacou vodou). Na stimuláciu čriev sa používajú aj lieky, ktoré zvyšujú motorickú aktivitu črevnej svalovej steny: 1 ml 0,05% roztoku prozerínu, intravenózne až 60 ml 10% roztoku hypertonického sodíka, až 500 mg ubretidy denne, hypertonický klystír 10-15 ml denne HBO). Spolu s načrtnutými metódami môže byť hyperbarická oxygenácia zahrnutá do boja proti črevnej paréze.
Hyperbarické okysličovanie zlepšuje tón a kontraktilitu črevnej steny (v súlade s Boyle-Mariottovým zákonom, objem intestinálnych plynov, keď sa zvyšuje vonkajší tlak, úmerne znižuje), t.j. kompresia v tlakovej komore vedie k dekompresii gastrointestinálneho traktu, ktorý urýchľuje difúziu plynu (dusík) z lúmenu čreva a periodická zmena tlaku v tlakovej komore (vzostup, výtok, opätovný vzostup, atď.) hrá úlohu mechanického stimulu k črevnej stene (podobne ako pôsobenie vodného kladiva počas klystýru). Zníženie objemu črevných plynov zlepšuje zásobovanie črevnej steny krvou, čo spolu so značným zvýšením okysličovania steny nielenže zvyšuje jej životaschopnosť a znižuje permeabilitu pre toxíny a baktérie, ale je tiež základom pre obnovenie peristaltiky. Bioelektrická aktivita črevnej steny je priamo závislá od veľkosti jej p02. Použitie HBO vám umožňuje odmietnuť opakované injekcie prozerínu a iných farmaceutických prípravkov, často s nežiaducimi vedľajšími účinkami.
Súbežne s kompenzáciou ťažkej hemodynamickej hypoxie (hypovolémia v dôsledku hojnej exsudácie do brušnej dutiny a črevného lúmenu, zvracania, ukladania krvi v cievach oblasti celiakie) a stabilizácie arteriálnej hypoxémie (hypoventilácia, venoarteriálny bypass atď.), Ktoré sú povinnými zložkami hypoxémie (hypoventilácia, venoarteriálny bypass, atď.), Ktoré sú povinnými zložkami hypoxémie, hypoventilácie, venoarteriálneho bypassu, atď. pozitívny účinok HBO v tejto patológii je do určitej miery spojený s priamym účinkom kyslíka na infekčný princíp a so zosilnením účinku antibiotika. v hypoxii, ako aj priaznivejší priebeh reparačných procesov v oblasti rany.
Mnohí pacienti po cisárskom reze majú problémy s močením a dokonca aj nemožnosť jeho implementácie. Ak sa moč nevylučuje, alebo ak sa vylučuje len málo, musí sa okamžite zistiť príčina tejto poruchy. Pri identifikácii funkčnej oligoanúrie sa zavádza princíp vyváženej nútenej diurézy. Dosahuje sa to intravenózne podávanie 20 až 40 mg furosemidu (lasix), opakované dávky liečiva sa podávajú tak, ako je uvedené. Príčinou retencie moču môže byť zle nainštalovaný alebo zablokovaný katéter, zakrivenie drenážnej trubice, krvná zrazenina atď. V takýchto prípadoch sa katéter a močový mechúr musia prepláchnuť antiseptickým roztokom pomocou injekčnej striekačky Janet.
V posledných rokoch sa v dôsledku zvýšenia počtu rezov cisárskym rezom pooperačné komplikácie stali veľmi dôležitými v štruktúre úmrtnosti matiek. A ak komplikácie ako krvácanie počas chirurgického zákroku a komplikácie spojené s anestéziou môžu byť minimalizované vysokou technológiou operácie, doplňovaním krvnej straty a adekvátnou anestéziou, riziko pooperačných komplikácií, najmä septiky, nemá tendenciu klesať v poslednom desaťročí. ,
Podľa N.Gleichera (1984) zvýšenie podielu cisárskeho rezu v USA o 1% zvýšilo riziko vzniku zápalových komplikácií v popôrodnom období 2-krát.
Najčastejšie sa po rezaní cisárskym rezom vyskytujú hnisavé-septické komplikácie, ktoré sú významným porodnickým problémom, pretože nemajú tendenciu znižovať a obsadiť jedno z prvých miest v štruktúre úmrtnosti matiek.
V štruktúre hnisavých-septických komplikácií prevláda endometritída, ktorá je hlavnou príčinou zovšeobecnenia infekcie a tvorby podradnej uterinnej jazvy.
Najhroznejšou hnisavou septickou komplikáciou je peritonitída. Napriek tomu, že v poslednej dobe je peritonitída relatívne zriedkavá, mortalita v tejto patológii zostáva vysoká a dosahuje 26-35%.
Jednou z metód prevencie vzniku infekcie po cisárskom reze je profylaktické použitie antibiotík. Ihneď po extrakcii plodu a upnutí pupočníkovej šnúry sa intravenózne injektuje 1 g širokospektrálnych antibiotík, po ktorých nasleduje podávanie 6, 12 alebo 12, 24 hodín Vysoká frekvencia a polyetiológia septických komplikácií po cisárskom reze určujú špeciálnu úlohu prevencie a liečby týchto komplikácií, v súčasnosti stále veľmi ďaleko od dokonalosti. Napriek veľkej pozornosti venovanej tomuto problému neexistujú jednotné zásady prevencie hnisavých-septických komplikácií. Niektorí autori napríklad uvažujú o použití antibiotík na boj proti infekčnej agresii, ktorá je vedúcou prevenciou v prevencii, zatiaľ čo iní uprednostňujú lieky a metódy, ktoré menia stav imunitného systému a zvyšujú obranyschopnosť organizmu zameranú na boj proti infekcii.
Je známe, že liečba endometritídy peritonitídy a iných hnisavých septických komplikácií závisí od úspešného riešenia dvoch kľúčových úloh; prevencia a liečba viacnásobného zlyhania orgánov a maximálna rehabilitácia brušnej dutiny.
Na vyriešenie týchto problémov je nevyhnutné: naliehavá reorganizácia hnisavého zamerania, podávanie antibakteriálnych liekov, liečivá na odstránenie zhoršenej hemodynamiky, detoxikačné prostriedky, zlepšenie funkcií vitálnych orgánov a stimulácia imunitnej reaktivity organizmu.
V prípade hnisavo-septických komplikácií, najmä peritonitídy, má najväčší význam infúzno-transfúzna terapia, ktorá sa vykonáva metódou kontrolovanej hemodilúcie s rozsiahlym použitím smerovo pôsobiacich krvných náhrad a roztokov s vyváženým iónovým zložením pod monitorovaným monitorovaním indikátorov koloidno-osmotického stavu.
Terapia začína zavedením roztokov koloidov s nízkou molekulovou hmotnosťou (reopolyglukín, gemodez). Tiež sa použili roztoky plazmy, albumínu, hmotnosti erytrocytov, etoxylovaného škrobu. Na zlepšenie hemodynamiky sú tiež podávané srdcové glykozidy, kortikosteroidy, ATP a prípravky na báze karboxylových kyselín.
Je to povinná liečba zameraná na elimináciu zhoršenej mikrocirkulácie a DIC; heparín 500 U / kg hmotnosť za deň, kyselina nikotínová 3 mg / kg, aminofylín 10 mg / kg, reopolyglukín 15 ml / kg, kontracal 100 000 U / kg.
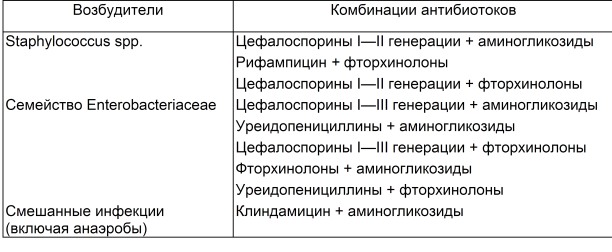
Vzhľadom na to, že peritonitída po reze cisárskym rezom je spôsobená mikrobiálnymi asociáciami, je potrebné použiť kombinovanú antibakteriálnu terapiu v kombinácii s liekmi, ktoré ovplyvňujú anaeróbnu flóru (tabuľka 4).
Kombinovaná liečba antibiotikami
Liečba hnisavých septických infekcií
Ako kritérium účinnosti antibakteriálnej liečby sa hodnotia hlavne klinické údaje, t. J. Zníženie telesnej teploty, pozitívne zmeny v hemogramu a urogramu, pokles Fi02 z 0,8-0,6 na 0,21 u pacientov s mechanickou ventiláciou a Synchronizácia pacienta s respirátorom je ďalším indikátorom adekvátnej antibiotickej liečby u pacientov s resuscitačným profilom.
Veľmi dôležitá je systematická mikrobiologická kontrola. Kritériá účinnosti liečby sú: eliminácia patogénu z hnisavého septického fokusu alebo z krvi po predchádzajúcom bakteriémii, čo znižuje stupeň kontaminácie mikróbov v rane. Pozitívnym faktom je zánik mikrobiálnych asociácií pri zachovaní jedného patogénu, ktorý je vysoko citlivý na rôzne antibakteriálne lieky.
Moderné metódy, ako napríklad plazmaferéza v kombinácii s ozónovou terapiou, sa v súčasnosti v širšej miere využívajú pri komplexnej terapii hnisavých septických komplikácií cisárskeho rezu, paretických stavov čreva. S vyššie uvedenými komplikáciami spravidla peritoneálny exsudát, prekrytie fibrínom, infikované krvné zrazeniny a devitalizované tkanivá slúžia ako živné médium pre mikroorganizmy a nie sú vždy dostupné antibiotikám a antiseptikám.
Plazmaferéza a ozónová terapia rozširujú možnosti terapeutických účinkov na systémovej a regionálnej úrovni. Je to spôsobené ich detoxikačnými, imuno-korektívnymi, re-korekčnými a baktericídnymi vlastnosťami.
Terapeutická plazmaferéza sa vykonáva v dvoch režimoch - prerušovane s použitím vakov Gemakon 500/300 a kontinuálne na separátore krvi „Vivacel 1“, „Haemonetics“ atď.
Technika prerušovanej plazmaferézy zahŕňa nasledujúce kroky:
1. Ulnárna žila je prepichnutá.
2. Začnite zavádzať plazmatický roztok. Množstvo roztoku podaného pred odberom krvi závisí od závažnosti stavu ženy, v priemere od 200 do 400 ml.
3. Vyrobte exfúziu krvi (400 ml) v plastových nádobách, ako napríklad „Gemakon 500/300“.
4. Pokračujte v zavádzaní roztokov nahrádzajúcich plazmu.
5. Oddeľte krvné bunky z plazmy v chladenej odstredivke (rýchlosť otáčania 4000 ot / min, čas 15 minút).
6. Plazma sa prenesie do satelitného vaku, krvinky sa zriedia 150 ml fyziologického roztoku a znovu sa premiešajú.
7. Postup sa opakuje 2-3 krát, čo vám umožní odstrániť 500-700 ml plazmy (bez hemokonzervatívu).
Priebeh liečby sa skladá z troch sedení plazmaferézy s intervalom 1-2 dni, po ktorom nasleduje ozónová terapia.
Hlavnými vlastnosťami ozónu, určujúcimi možnosť jeho použitia pri prevencii a liečbe hnisavých-septických komplikácií, sú jeho baktericídne a antivírusové účinky.
Mechanizmus baktericídneho pôsobenia ozónu je pre neho priepustnosť biomembrán. V dôsledku toho sú plazmové membrány primárnym cieľom biocídneho účinku ozónu. Priama príčina smrti baktérií pôsobením ozónu je lokálne poškodenie plazmatickej membrány, čo má za následok stratu životaschopnosti bakteriálnej bunky a / alebo jej schopnosť reprodukcie. Ozón má chemicky neutralizujúci účinok na mikrobiálne toxíny.
Významný je trofický účinok na výživu buniek. Je to spôsobené zvláštnosťou ozónových molekúl, ktoré prenášajú väčšinu energie, ktorá je v nich obsiahnutá, od momentu vzniku.
Ozón významne ovplyvňuje priebeh zápalového procesu: na jednej strane znižuje účinky stresu, má analgetický účinok; na druhej strane reguluje priebeh obranných reakcií, čím znižuje deštrukčnú fázu zápalu, ktorá zase zabraňuje zjazveniu.
Keď je ozón vystavený krvi, dramaticky sa zvyšuje parciálny tlak kyslíka a extra-intracelulárne a redox procesy spojené s produkciou a využívaním energetických substrátov, konverziou a syntézou biologicky aktívnych látok (katecholamíny, serotonín, histamín, atď.) Sú zvýšené. Súčasne dochádza k zvýšeniu aktivity imunokompetentných periférnych krvných buniek so zahrnutím endogénnych detoxikačných mechanizmov (využitie oxidovaných produktov, regenerácia pH, redukcia v krvi konečných produktov metabolizmu dusíka, normalizácia funkcie pečene, obličiek a pľúc).
Priebeh ozónovej terapie pre septické komplikácie zahŕňa 5 procedúr a prvý deň sa vysoké koncentrácie 4-5 mg / l ozónu používajú v 400 ml 0,9% roztoku chloridu sodného intravenózne raz denne. Počas 2. a 3. postupu je koncentrácia ozónu 3 mg / lv 400 ml 0,9% roztoku chloridu sodného intravenózne raz denne. Počas 4. až 5. postupu je koncentrácia ozónu 2 mg / lv 400 ml 0,9% roztoku chloridu sodného intravenózne raz denne.
Endovaskulárne laserové ožarovanie krvi (ELOK) je vysoko účinnou metódou na liečbu hnisavých septických komplikácií v pooperačnom období.
Laserový účinok na krv spôsobuje analgetické, imunokorekčné, antibakteriálne, anti-edémové a protizápalové účinky. V tomto ohľade sa laserový efekt účinne používa na prevenciu a liečbu hnisavých septických komplikácií.
Na základe mnohých klinických údajov sa zistilo, že v dôsledku pôsobenia laserového žiarenia na krv dochádza v tele k zmenám, ktoré sa realizujú primárne na subcelulárnej, potom bunkovej, tkanivovej, systémovej a orgánovej úrovni. Hlavným účinkom laserového žiarenia na krv je zmena aktivity redox procesov na subcelulárnej úrovni.
Purulentné septické ochorenia sú sprevádzané deštruktívnymi procesmi v centre pozornosti a rozvojom endogénneho intoxikačného syndrómu v tele. Zníženie produktov deštrukcie tkaniva po laserovej terapii indikuje pokles zápalového procesu, v dôsledku čoho sa znižuje hladina endogénnej intoxikácie v tele.
Dôležitým účinkom ELOK je zlepšenie mikrocirkulácie, v dôsledku čoho sa zvyšuje prísun kyslíkových substrátov do miesta zápalu a CBS a krvné plyny sa normalizujú.
Použitie laserovej terapie má pozitívny vplyv na systém zrážania krvi (redukcia fibrinogénu, ITP), čo významne znižuje riziko tromboembolických komplikácií.
ELC sa vykonáva pomocou inštalácie ULF-01 a ADEPT. Na intravaskulárne ožarovanie krvi sa cez ihlu vpichu vloží do ulnárnej žily monofilné kremenné vlákno. Trvanie procedúry je 15-30 minút. Liečba sa vykonáva raz denne, kurz je 7-10 sedení.
V neprítomnosti venózny prístup vykonávať neinvazívne laserové ožarovanie vystavením cievneho zväzku stehennej kosti v oblasti slabín. Výkon žiarenia je 35-140 mW, trvanie procedúry je 15-30 min. Liečba sa uskutočňuje raz denne počas 7-10 sedení.
Hlavnými pozitívnymi účinkami použitia týchto metód na pooperačné komplikácie sú potlačenie adhézneho procesu, výrazné fibrinolytické a nekrolytické účinky, zníženie výskytu viacnásobného zlyhania orgánov a zlepšenie výsledkov liečby pacientov s pooperačnými komplikáciami.
Časté a nebezpečné komplikácie abdominálneho podávania sú krvácanie, ich frekvencia je 3-5 krát vyššia ako po spontánnom pôrode. Krvácanie po reze cisárskym rezom sa vyvíja na začiatku aj v neskorom pooperačnom období.
Liečba krvácania by mala byť včasná, komplexná a mala by zahŕňať všeobecné princípy intenzívnej terapie, ako sú: katetrizácia jednej alebo dvoch hlavných žíl, hodinové monitorovanie CVP, diuréza; stanovenie parametrov koncentrácie v krvi (hemoglobín, hematokrit, počet červených krviniek).
Pri krvácaní v skorom pooperačnom období by ste mali využiť možnosť zastaviť krvácanie konzervatívnymi prostriedkami, ktoré zahŕňajú:
Včasné vyprázdnenie močového mechúra,
Vonkajšia masáž maternice,
Intravenózne podávanie uterotonických látok (oxytocín, metylergometrín, prostaglandín),
Manuálne alebo inštrumentálne vyprázdňovanie maternice (s nasadenou operačnou sálou a intravenóznou anestéziou s kalipsolom), \\ t
Zavedenie uterotonických látok do krčka maternice,
Infúzna transfúzna terapia (čerstvá zmrazená plazma, hmotnosť erytrocytov, kyselina transaminová atď.).
Účinnosť tejto liečby je podľa našich údajov 82,4%.
V neprítomnosti účinku a so závažným DIC sa niekedy uchyľujú k ligácii vnútorných ileálnych artérií.
Normalizácia hemodynamiky by mala začať infúznou-transfúznou liečbou. Základom liečby je obnova systémovej hemodynamiky zavedením roztokov s vysokou molekulovou hmotnosťou. Prostriedkami voľby v tomto prípade sú liečivá etoxylovaného škrobu (6 a 10% HAES Steril, Infukol HAS) v množstve 10 až 20 mg / kg / hod, volekama od 500 do 1000 ml. Hemodynamický účinok týchto liečiv je 2-3 krát vyšší ako účinok roztoku albumínu s trvaním hemodilučného účinku 4-6 hodín.
Vzhľadom na vývoj hypoglykémie s masívnou stratou krvi sa odporúča zahrnúť do infúzno-transfúznej terapie roztoky koncentrovaných sacharidov (10 a 20%). Zavedenie roztokov glukózy nielen prispieva k obnoveniu energetických zdrojov, ale tiež potencuje hemodynamický účinok etoxylovaného škrobu. Na korekciu hemokoagulačného potenciálu a obnovenie onkotickej rovnováhy je potrebná transfúzia čerstvej zmrazenej plazmy v dávke 15 ml / kg telesnej hmotnosti. Obnovenie globulového objemu erytromasovou transfúziou (nie viac ako 3 dni skladovania) alebo zavedenie 400-500 ml erytropoetínu sa uskutočňuje len vtedy, ak je hladina hemoglobínu nižšia ako 80 g / l, hematokrit je menší ako 25 l / l. V pooperačnom období často nastáva otázka liečby anémie. Liečba prípravkami železa je spravidla dlhodobá a má vedľajšie účinky (najčastejšie z gastrointestinálneho traktu) a v niektorých prípadoch neúspešne. Transfúzia krvi sa vykonáva v ojedinelých prípadoch a len podľa životne dôležitých indikácií. V súčasnosti by sa liečba anémie ľudským rekombinantným erytropoetínom mala považovať za alternatívu k tradičnej terapii. Erytropoetín je glykoproteínový hormón, ktorý reguluje erytropoézu, ktorá zvyšuje tvorbu červených krviniek. V tejto súvislosti je v pooperačnom období s anémiou nevyhnutné používať erytropoetín v dávke 60 U / kg raz denne intravenózne počas 5 dní. Táto terapia by sa mala vykonávať na pozadí liečby glukokortikoidmi a zavedením inhibítorov proteolýzy, ktoré sa považujú za ochrancov šoku a normalizujú procesy hemokoagulácie. Normalizácia mikrocirkulácie sa uskutočňuje zavedením protidoštičkových činidiel (trental, reopolyglukine).
Krvné transfúzie a podávanie plazmy sa majú vykonávať s povinným použitím filtrov. V posledných rokoch sa výrazne zvýšilo používanie filtrov na transfúziu krvi a jej zložiek. Je známe, že agregácia krvných doštičiek nastáva v priebehu niekoľkých hodín od uskladnenia krvi. Leukocyty strácajú svoju aktivitu a postupne sa spájajú s lepenými doštičkami. Následne usadené fibrínové filamenty upevňujú vytvorený konglomerát a dokončujú proces vytvárania stabilného mikroagregátu. Prenikanie mikroagregátov do krvného obehu je spojené s rozvojom mnohých komplikácií. Predovšetkým infúziou krvi je možná oklúzia prevalilárnych pľúcnych arteriol. Okrem toho zložky mikroagregátov môžu iniciovať uvoľňovanie biochemicky účinných látok, čo zasa prispieva k rozvoju syndrómu respiračnej tiesne (RDS). Faktory predisponujúce k rozvoju RDS u pôrodných pacientov môžu zahŕňať:
1. Predĺžený chirurgický zákrok (cisársky rez + myomektómia, súvisiace abdominálne nádory).
2. Počiatočná anémia vyžadujúca krvné transfúzie.
3. DIC syndróm.
4. Aspirácia obsahu žalúdka.
5. Bakterémia (chorioamnionitída, placentitída atď.).
6. Zápalové ochorenia pľúc, genitálie.
7. Extragenitálna patológia (pyelonefritída, ochorenie pečene atď.)
Kombinácia dvoch alebo viacerých predispozičných faktorov dramaticky zvyšuje pravdepodobnosť vzniku syndrómu respiračnej tiesne a zhoršuje prognózu pre pacienta počas transfúzie krvi. Jednou z možností, ako sa vyhnúť komplikáciám počas transfúzie krvi a jej zložiek, je použitie mikroagregátových filtrov Pall Biomedical. Je známe, že po transfúzii 3 až 4 krvných jednotiek s použitím štandardného filtra (priemer pórov 170 um, sa zadržia len dostatočne veľké zrazeniny) sa vyvíja trombocytopénia, ktorá sa nedá vysvetliť len hemodilúciou. Toto je zvlášť dôležité u žien s počiatočnou trombocytopéniou. Ďalšou zložkou krvnej plazmy, ktorej koncentrácia a aktivita klesá po transfúzii krvi, je fibronektín, čo je glykoproteín, ktorý má opsonínovú aktivitu a podporuje zachytávanie baktérií a cudzích telies retikuloendotelovým systémom. Toto je zvlášť dôležité u žien s autoimunitnými poruchami a imunodeficienciou.
So zvyšujúcim sa obdobím skladovania krvi sa zvyšuje koncentrácia histamínu, ktorý je obsiahnutý v bazofilných granulocytoch, ktoré sú jednou zo zložiek mikroagregátov. U 1-2% pacientov liečených transfúziou sa vyskytujú nehemolytické febrilné reakcie, ktoré sa často vyskytujú u pacientov s B-talasémiou. Klinicky sa to prejavuje: horúčkou, zvýšenou srdcovou frekvenciou, zimnicou. Použitie týchto filtrov môže významne znížiť závažnosť post-transfúznej trombocytopénie, znížiť množstvo histamínu podávaného zvonka krvou a incidenciu HHFR o 77%.
Potenciálnym problémom pri transfúzii krvi je výskyt aloimunizácie cudzích HLA antigénov, najmä u pacientov s krvnými ochoreniami. Samotné červené krvinky, krvné doštičky a granulocyty nemôžu spôsobiť aloimunizáciu, pretože sú cieľom antigénov HLA triedy II. Produkcia protilátok HLA vyžaduje bunky nesúce antigény HLA triedy I a antigény HLA triedy II. Všetky nukleové bunky a krvné doštičky majú antigény HLA triedy I, antigény triedy II sú prítomné len na povrchu monocytov, makrofágov, B lymfocytov a aktivovaných T lymfocytov, ktoré sa nazývajú bunky prezentujúce antigén (APC) a sú zodpovedné za procesy aloimunizácie (obrázok č. . 3).
Použitie filtrov znižuje výskyt týchto komplikácií, ako aj prenos ľudského lymfotropného vírusu T-buniek (HTLV-1), vírusu Epstein-Barrovej, HIV, hepatitídy a zabraňuje rozvoju cytomegalovírusovej infekcie.
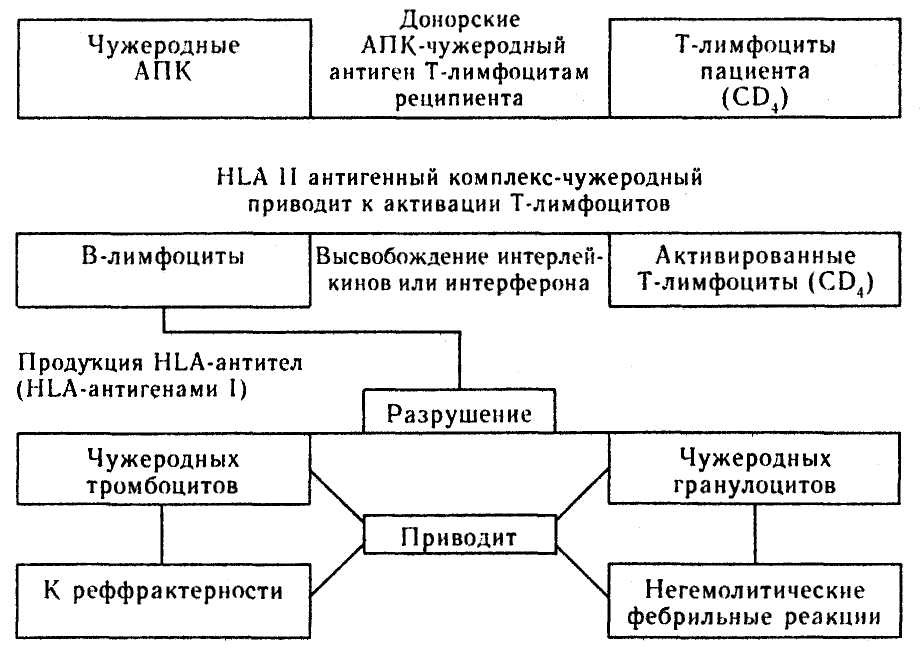
Obr. 3. Mechanizmus aloimunizácie HLA a následné klinické prejavy krvnej transfúzie.
Pri neefektívnosti tejto liečby je potrebné vyvinúť pacienta s viacnásobným zlyhaním orgánov, pričom je potrebné použiť eferentné metódy.
Plazmaferéza sa uskutočňuje v prvých hodinách po dosiahnutí chirurgickej hemostázy. Súčasne sa vylúči najmenej 70% VCP s primeranou kompenzáciou donorovej čerstvej zmrazenej plazmy. Táto technika, s jej včasnou implementáciou vám umožňuje úplne eliminovať rozvoj syndrómu viacnásobného zlyhania orgánov. Správne a včasné vykonanie infúzno-transfúznej terapie v kombinácii s eferentnými metódami môže významne zlepšiť výsledky terapie a zabrániť mortalite počas tejto komplikácie.
Tromboembolické komplikácie - jedna z troch hlavných príčin úmrtnosti matiek, patria medzi najnebezpečnejšie pôrodnícke komplikácie. Riziko ich vývoja po cisárskom rezu je 10-15 krát vyššie ako po pôrode cez prirodzený pôrodný kanál a dosahuje 8,5%. Miera úmrtnosti matiek je 1 -1,6 na 10 000 pôrodov.
U zdravých žien je hemostatický proces normálnou reakciou tela na tehotenstvo, pôrod a operáciu.
Riziko pooperačných tromboembolických komplikácií sa zvyšuje dramaticky u tehotných žien s extragenital patológie, komplikácie tehotenstva a zaťažené pôrodníckej anamnézy (kardiovaskulárne choroby, anémia, ochorenia obličiek, diabetes, neskoré gestózou, potraty, maternicové myómy, kŕčové žily, antifosfolipidové syndróm, a tak ďalej. d.).
Existuje mnoho dôvodov, ktoré môžu viesť k trombóze. Patrí medzi ne poškodenie cievnej steny, hemodynamické poruchy, zhoršené dýchacie funkcie, hemostázový systém.
Medzi vaskulárne faktory priamo súvisiace s trombózou patria prostacyklíny, relaxačný endotelový faktor, endotel, plazminogénny aktivátor tkanivového typu, produkt metabolizmu lipidov - kyselina 13-hydroxyoktadekadiénová, heparín atď. Teda, cievna stena hrá dôležitú úlohu pri zabezpečovaní hemostatických reakcií ,
V tele zdravej ženy, bez ohľadu na spôsob podávania, ktorý spôsobil integritu alebo funkčnú aktivitu vaskulárnej steny, je iniciovaný proces zameraný na prevenciu a redukciu závažnosti hemoragických porúch a na obmedzenie procesov tvorby trombov.
Komplikácie tehotenstva, pôrodu, extragenitálnej patológie, krvácania, popôrodných komplikácií vedú k nerovnováhe protrombogénnych a antitrombogénnych vaskulárnych faktorov, čím prispievajú k posilneniu vlastností zrážania krvi.
Faktor, ktorý prispieva k zvýšeniu zrážanlivosti krvi, je vstup plodovej vody počas operácie do brušnej dutiny. Ľahko sa vstrebávajú a prispievajú k hyperkoagulácii krvi.
Hemodynamické poruchy, dysfunkcie respiračného systému, hemostáza môžu tiež vyvolať tvorbu trombov, ktoré ovplyvňujú nielen funkčnú aktivitu endotelových buniek a krvných doštičiek, ale tiež zvyšujú reakcie plazmatickej väzby hemostázy a adhézie krvných doštičiek.
Príčinou tromboembolických komplikácií môže byť zmena obsahu fibrinogénu, proteínu C, faktora V, výskyt protilátok proti fosfolipidovým komplexom v krvi, nedostatok faktora XII atď.
Pri prevencii tromboembolických komplikácií u tehotných žien, pôrodných žien a šestonediel sa musia zohľadniť nasledujúce rizikové faktory, ktoré prispievajú k tomuto typu komplikácií. Patrí medzi ne:
1. Autoimunitné a infekčné imunitné ochorenia (APS, alergické ochorenie, trombovaskulitída, hnisavé zápalové ochorenia atď.);
2. Krvné ochorenia (hemorheologické formy - polycytémia, paraproteinémia, trombocytémia, hypertrombocytóza, poškodenie cievnych doštičiek atď.);
3. Extragenitálna patológia (diabetes, srdcové ochorenia, hypertenzia, obličky, pečeň, dedičná hyperlipidémia atď.);
4. Závažné formy gestazy, obvyklé potraty atď.
Spontánna trombóza v pooperačnom období je možná s masívnou stratou krvi, výskytom viacnásobného zlyhania orgánov, hnisavými septickými komplikáciami. Okrem toho je potrebné vedieť, že počas tehotenstva je možný rozvoj trombózy v akomkoľvek trimestri, najmä u žien s femorálnou trombózou, ktorí užívajú perorálne kontraceptíva po dlhú dobu, prítomnosť syndrómu APS atď.
Dôležitú úlohu pri rozvoji venóznej a arteriálnej trombózy zhoršujú reologické vlastnosti krvi, a to zvýšenie viskozity, polyglobulie, polycytémie - s vysokou hladinou hematokritu, hemoglobínu, erytrocytov, krvných doštičiek, zrýchleného ESR, zvýšeného obsahu fibrinogénu.
Nedostatočnosť hlavných fyziologických inhibítorov koagulácie alebo ich kofaktorov (antitrombín III, heparínový faktor II, proteín C, S, inhibítor komplexu faktora VIla) môže tiež viesť k rozvoju trombózy. Zníženie ich hladiny možno pozorovať u žien s ochorením pečene, sepsou, cukrovkou, dlhodobou terapiou heparínom atď.
Pomerne často je trombóza spôsobená zápalovými komplikáciami, ktoré sa vyskytujú v období po pôrode. Hlavným dôvodom je prítomnosť endotoxínu v krvi a uvoľňovanie cytokínov z buniek.
Pomerne často je hematogénna trombofília spôsobená nedostatkom a abnormalitami proteínu C, nedostatkom antitrombínu III, ktorý blokuje aktivitu trombínu, faktorom IXa, Xa, XI. V prítomnosti heparínu sa dramaticky zvyšuje účinok antitrombínu. Nedostatok týchto faktorov môže byť primárny alebo sekundárny.
Dedičná forma je autozomálne dominantne dedičné ochorenie. To inhibuje syntézu prírodných antikoagulancií. Výskyt protilátok proti fosfolipidovým komplexom v krvi (lupus antikoagulant) môže tiež viesť k tejto komplikácii. Súčasne sa trombofília vyskytuje na pozadí DIC pri dlhodobom používaní heparínu, pričom sa užívajú syntetické progestíny.
Inhibícia fibrinolýzy sa môže vyvinúť pod vplyvom pôsobenia silných inhibítorov aktivátorov plazminogénu a plazmínu, ktoré sa často vyskytujú pri gestose, v krvi.
Nedostatok plazminogénu môže byť tiež príčinou trombózy pri systémovej vaskulitíde, syndróme DIC, ako aj pri podávaní veľkých dávok aktivátorov plazminogénu a defibrinujúcich liekov.
S výskytom imunitných komplexov v krvi, aktivovaných zložiek komplementového systému, je možné zvýšiť adhezívne agregačnú aktivitu krvných doštičiek, vzhľad aktívnej plazmatickej formy glykoproteínu, ktorý sa často vyskytuje počas glomerulonefritídy, akútnych infekcií, sepsy, šoku atď.
Na prevenciu hematogénnej trombofílie je preto potrebné zvážiť rizikové faktory.
Najvýraznejšou tromboembolickou komplikáciou je pľúcna embólia.
Ak je podozrenie na tromboembolizmus pľúcnej artérie, je potrebné podať intravenózne 10 000 až 50 000 IU heparínu. Po diagnostike sa tromboembolická terapia vykonáva 2-3 dni (streptase, streptokináza v dávke 2 000 000 - 3 500 000 U).
Heparín sa v prvých dvoch dňoch podáva intravenózne v dávke 30 000 - 50 000 IU s reopolyglucínom, potom subkutánne pod kontrolou ukazovateľov hemostasiogramu.
Heparín je pomerne ťažké použiť na liečenie a prevenciu trombózy po dlhú dobu kvôli možnosti hemoragických komplikácií. Preto, keď je potrebná dlhodobá antitrombotická liečba, je potrebné použiť nepriamo pôsobiace antikoagulanciá (dikoumarín, marcumar, fenilín atď.), Ktoré nezabraňujú tvorbe zrazeniny priamym kontaktom s krvou alebo plazmou a ich účinok je spôsobený znížením plazmatickej hladiny - faktorov závislých od vitamínu K - II, VII, IX, X.
Účinnosť liečby sa monitoruje stanovením koncentrácie fibrinogénu, trombínového času, angiopulmonografie a rádiografie pľúc.
Prevencia tromboembolických komplikácií po cisárskom reze zahŕňa včasnú detekciu a liečbu extragenitálnych ochorení a komplikácií tehotenstva s chronickou formou DIC, mikrocirkulačných porúch. Niektorí autori v tejto kategórii pacientov odporúčajú podávanie počas chirurgického zákroku, po prešití rany do maternice, jednorazovú dávku heparínu intravenózne (5-10 U). Kontrola účinku heparínu sa vykonáva podľa času zrážania krvi s výpočtom heparínového koeficientu. Podľa E.Clementa (1990) takáto prevencia môže znížiť výskyt pooperačných tromboembolických komplikácií z 1,1 na 0,34%. V tejto štúdii sa heparín podával nielen ženám s vysokým rizikom vzniku týchto komplikácií, ale aj všetkým tehotným ženám a matkám počas cisárskeho rezu.
Embolizmus amniotickej tekutiny alebo amniotická embólia je jednou z najnebezpečnejších pôrodníckych komplikácií, ku ktorej dochádza častejšie ako je diagnostikovaná.
Úmrtnosť v tejto patológii je 86%. Ak vezmeme do úvahy, že v niektorých prípadoch smrteľná amniotická embólia nepochybne prechádza pod inými diagnózami, potom sa nebezpečenstvo tejto patológie ešte viac prejaví.
Amniotická embólia sa pozoruje vo forme dvoch hlavných syndrómov - kardiopulmonálneho šoku a koagulopatického krvácania. Prvý syndróm sa vyskytuje v 60-70% prípadov amniotickej embólie, a ak pacient zostane nažive, druhý syndróm sa takmer vždy pripojí.
Je dokázané, že plodová voda nikdy nevstúpi prirodzeným spôsobom do krvného obehu. Aby sa to stalo, sú potrebné aspoň dve podmienky - prevaha amniotického tlaku na žilový tlak a otvorenie žilových ciev maternice.
Lymiotický tlak sa stáva častejšie ako venózny najčastejšie na pozadí hypovolémie akéhokoľvek genézu. V dôsledku toho je operácia cisárskeho rezu, ktorá poskytuje druhú podmienku (otvorenie žilových ciev maternice) u žien s patológiou tehotenstva a sprievodnou hypovolémiou, plná rizika amniotickej embólie.
S rozvojom kardiopulmonálneho šoku je intenzívna terapia najčastejšie jednotkou intenzívnej starostlivosti. Opatrenia resuscitácie možno rozdeliť do troch skupín:
1) udržiavanie dýchania, krvného obehu a metabolizmu umelými prostriedkami;
2) prerušenie reflexných reakcií tanatogenézy;
3) eliminácia následkov kardiopulmonálneho šoku.
Včasný nástup resuscitácie je kľúčom k úspešnému výsledku, pretože s bleskovou formou amniotickej embólie majú pacienti tendenciu rýchlo umrieť a čím kratšie obdobie umierania, tým väčšia nádej na úspešnú reanimáciu a rehabilitáciu.
Čo sa týka reflexných mechanizmov tanatogenézy, je možné, že sú eliminované klinickou smrťou a resuscitáciou. Koniec koncov, srdce sa zastaví kvôli tomu, že agresívne látky, zadržané pľúcnym kapilárnym filtrom, spustili komplexný reťaz reakcií. Pri mechanickej masáži srdca a mechanickej ventilácii sa táto vysoká koncentrácia plodovej vody zriedi krvou a viac-menej rovnomerne rozloží po celom tele.
Pretože iniciátorom nežatogénnych reakcií je PG F2a, možno použiť antiprostaglandínové činidlá (kyselina acetylsalicylová, indometacín atď.). Okrem toho sa intravenózne podávajú neuroleptiká, analgetiká a heparín. Neuroleptanalgetika prerušuje reflexné reakcie, stabilizuje vegetatívne funkcie, odstraňuje strach, bolesť, katecholaminémiu, to znamená spôsobuje srdcovú fibriláciu komôr. Heparín sa používa nielen ako antikoagulačné činidlo prerušujúce ICE, ale aj ako antagonista serotonínu.
Na zmiernenie bronchiolospazmu a zlepšenie mikrocirkulácie krvi sa intravenózne podáva alupent, aminofylín a retrosternálna blokáda sa uskutočňuje s roztokom 0,25% novokaínu (50-100 ml).
Akútna hypovolémia sa eliminuje infúziou reopolyglukínu, ktorý súčasne zabraňuje vzniku DIC, permanentnej zložky amniotickej embólie v niektorom z jej variantov.
Eliminácia následkov kardiopulmonálneho šoku spočíva v eliminácii metabolickej acidózy, stimulácii diurézy na prevenciu akútneho zlyhania obličiek, pri aplikácii režimu so zvýšeným tlakom na konci výdychu, a to tak s umelým, ako aj spontánnym vetraním pľúc, aby sa zabránilo ich tendencii k atelektácii spojenej s amniotickou embóliou ,
Na liečenie tejto patológie sa teraz môžu úspešne použiť metódy eferentnej chirurgie krvi (výmena plazmy, plazmová filtrácia). Ich použitie je patogeneticky odôvodnené, pretože účinok je spôsobený takými mechanizmami, ako sú odstraňovanie toxických látok, autoprotilátok, imunitných komplexov, metabolických produktov, zložiek zničených tkanív a buniek z krvného obehu, rýchla eliminácia hypovolémie a zlepšenie mikrocirkulácie.
Osobitnú pozornosť si vyžaduje manažment pacientov s preeklampsiou, najmä s ťažkými formami (eklampsia, HELLP syndróm), ktoré najčastejšie spôsobujú takéto pooperačné komplikácie, ako je krvácanie a tromboembolizmus.
Jedným z prejavov závažných foriem preeklampsie je HELLP syndróm (hemolýza, zvýšená aktivita pečeňových enzýmov a trombocytopénia). Včasné klinické príznaky HELLP syndrómu môžu byť nevoľnosť, vracanie a opuch v hornej časti brucha. Značená trombocytopénia nižšia ako 100 109 / l. Spojenie HELLP syndrómu poukazuje na extrémny stupeň nesprávnej adaptácie telesných systémov matky. V závažných prípadoch to vedie k rozvoju intravaskulárnej koagulácie a závažnému pôrodníckemu krvácaniu.
Eklampsia je najzávažnejšou formou neskorej gestazy. Eklampická kóma je obzvlášť nebezpečná, keď má žena narušené vedomie aj mimo kŕčovitého záchvatu. S touto patológiou koniec operácie neznamená koniec anestézie. Pri eklampsickom kóme alebo eklampsickom stave v pooperačnom období sa vykonáva dlhotrvajúca umelá ventilácia pľúc až do stabilizácie hlavných parametrov homeostázy.
Indikácie mechanickej ventilácie sú: neprítomnosť alebo narušenie vedomia mimo záchvatov, arteriálna hypertenzia nie je vyriešená konvenčnou antihypertenzívnou liečbou, konvulzívna pripravenosť nie je eliminovaná konvenčnou antikonvulzívnou terapiou.
Mechanické vetranie sa spravidla musí vykonávať v režime výraznej hyperventilácie (s PaCO2 20-22 mmHg). Len tak je možné dosiahnuť prispôsobenie pacientov respirátoru. Ťažkou úlohou je často eliminácia ťažkej hypoxémie, preto sa odporúča zvýšiť tlak do konca expirácie (voda 10-12 cm.). Na pozadí mechanickej ventilácie sa vykonáva masívna sedatíva, antikonvulzíva a antihypertenzívna liečba (seduxen, neuroptan-algetic).
V prípade pretrvávajúcej arteriálnej hypertenzie sa používajú ganglioblockery (pentamín 0,5-1,5 ml 5% roztoku intravenózne). U jednotlivých pacientov nemusia mať ani ganglioblockery hypotenzný účinok a účinok má len viaczložková komplexná liečba.
Treba však poznamenať, že „intenzívna“ terapia v tejto patológii neznamená veľa a vo veľkých množstvách. V prvom rade ide o intenzívne myslenie lekára, ktorý podľa stavu pacienta priradí primerane minimálne množstvo liečby s minimálnym počtom vedľajších účinkov a následkov.
Popri opísanej terapii, použití plazmaferézy spolu s infúziou proteínových prípravkov, fyziologických roztokov, sú vysoko účinné preparáty reologického pôsobenia. Je potrebná dôkladná korekcia všetkých metabolických porúch v dennej biochemickej analýze krvi a moču. Veľmi dôležitá je najmä v prípade pľúcnych komplikácií eliminácia hyperkoagulácie podávaním heparínu. Na zníženie permeability cievnej steny sa odporúča prevencia a liečba edému mozgu, hydrokortizónu (500-800 mg denne) alebo prednizónu (90-60 mg denne).
Treba venovať pozornosť tzv. Dehydratačnej terapii (saluretiká, osmotické látky). Sú neefektívne, prehlbujú porušovanie rovnováhy vody a elektrolytov, často vyvolávajú zvýšenie záchvatového syndrómu, najmä ak sa podávajú na pozadí zvýšeného osmotického tlaku plazmy.
Mechanickú ventiláciu je možné ukončiť u pacientov s eklampsiou len v neprítomnosti konvulzívnych záchvatov a konvulzívnej pripravenosti bez použitia antikonvulzív a sedatívnej terapie počas 3 dní. Druhým predpokladom je absencia pľúcnych komplikácií.
Prenos pacientov na spontánne dýchanie by mal byť postupne pod dohľadom klinického laboratórneho výskumu podľa všetkých pravidiel resuscitačnej techniky.
Veľmi dôležitá je pooperačná fyzioterapia a fyzioterapia. Pred operáciou sa odporúča, aby tehotná žena cvičila niekoľko cvičení. Po operácii, nasledujúce cvičenia:
1. Dýchacie cvičenia: pacient sa zhlboka nadýchne nosom a vydýchne ústami. Toto cvičenie sa vykonáva 5-krát počas každej hodiny pod dohľadom metodika. Hlavným cieľom dychových cvičení je obnova diafragmatického dýchania, ktoré je dočasne narušené po operáciách brucha.
2. Pomoc pacientovi s kašľom: sestra jemne pritláča ruky na bruchu na oboch stranách rany. Potom môže pacient vykašľať bez nepohodlia.
3. Aktívne pohyby. Vykonáva sa na zlepšenie periférnej cirkulácie, aby sa zabránilo rozvoju tromboflebitídy. Pacient vykonáva nasledujúce cvičenia: každú hodinu sa ohýba 5-krát a narovná nohy na kolenách a 5-násobne ohne a uvoľní nohy, voľne a pri vytváraní prekážok. V prípade pooperačného krvácania sa s veľkou opatrnosťou vykonáva respiračná gymnastika a aktívne pohyby. Ak má pacient kašeľ, sú potrebné špeciálne opatrenia.
4. Zapnutie na boku, aby sa zabránilo tromboflebitíde a preležaninám, ako aj na zlepšenie krvného obehu. Metodista jednou rukou podopiera pacienta ramenami, druhý za chrbtom a pomáha jej prevrátiť sa na boku, až kým sa pacient necíti pohodlne v novej pozícii v posteli.
5. Pomoc pacientovi pri výstupe z postele: pacient sa otočí na bok a vstane, opiera sa o pravý lakeť a ľavú ruku, ak sa otočí na pravej strane a na ľavom lakte a pravej paži, ak sa otočí na ľavej strane. Potom metodik alebo zdravotná sestra oddelenia kladie ruky pod hlavu a ramená pacienta a pomáha jej pomaly sedieť na posteli a znížiť nohy. Pacientka nejakú dobu sedí na okraji postele, keď spustila nohy, potom vstane a urobí niekoľko krokov, metodik jej starostlivo pomôže.
Diéta od prvého dňa po cisárskom rezu obsahuje vývar, želé, krupicu, z druhého dňa tabuľky číslo 10 je predpísané, od 3-4 deň - spoločný stôl. Potraviny by mali byť vysokokalorické, vysoko kvalitné a rozmanité s dostatočným množstvom bielkovín a rastlinných vlákien.
Na zhodnotenie pooperačného obdobia sa okrem klinického pozorovania používajú aj štúdie s použitím štandardných metód (klinická analýza krvi a moču, biochemická analýza krvi, hemostasiogram). Ultrazvukové vyšetrenie maternice s hodnotením jeho involúcie a echo-špecifických zmien v oblasti stehov sa vykonáva na 5. až 6. deň. Podľa ultrazvuku je normálna expanzia maternice na 1-1,5 cm.
Nepriaznivým znakom je prítomnosť plynu v maternici a v pooperačnej oblasti stehu.
Pri zisťovaní akýchkoľvek patologických zmien (ukladanie fibrínu, expanzia maternice atď.) Je potrebné použiť uterotonické činidlá s antispazmodikami. Pri nepriaznivom bakteriologickom pozadí sa používa drenáž odsávaním maternice. Po odstránení po narodení sa v priebehu chirurgického zákroku zavedie do dutiny maternice trubica vinylchloridu v tvare T alebo O v tvare vinylu s viacerými otvormi, pozdĺžny koniec trubice sa vytiahne cez kanál krčka maternice a pošvy, vyberie sa a fixuje stehom do krčka maternice.
Do 4-5 dní, 1-2 krát denne, odsajte obsah maternice a potom zavlažujte 20 ml 1% roztoku dioxidínu. Dojčenie v neprítomnosti kontraindikácií je povolené 3. deň po operácii. V prípade komplikovaného pooperačného obdobia, spolu s pevným bandážovaním prsných žliaz, sa parlodel (bromokriptín) predpisuje 2,5 mg 2-krát denne. Kontraindikácia na jeho použitie je hypotenzia, srdcové arytmie, ochorenia gastrointestinálneho traktu.
Druhý deň po operácii sa pooperačný steh ošetrí 70% alkoholom, potom brilantnou zelenou alebo 10% roztokom manganistanu draselného. Po zaschnutí pokožky sa čiary švov postriekajú 3-krát filmom fusilu na ochranu švíkov pred infekciou až do ich odstránenia 7. dňa.
Po odstránení stehov sa lifusol odstráni tampónom navlhčeným éterom alebo alkoholom.
Treba upozorniť čitateľa na skutočnosť, že len včasné a komplexné uplatňovanie všetkých princípov intenzívnej terapie spoločne všetkými klinickými a laboratórnymi oddeleniami zdravotníckeho zariadenia umožní dosiahnuť najväčší úspech v prevencii a liečbe pooperačných komplikácií.
Pooperačné obdobie - obdobie od skončenia operácie po zotavenie alebo úplnú stabilizáciu stavu pacienta. Je rozdelená na najbližšiu - od okamihu ukončenia operácie až po vypustenie a vzdialenú, ktorá sa nachádza mimo nemocnice (od prepustenia až po úplnú elimináciu všeobecných a lokálnych porúch spôsobených chorobou a operáciou).
Všetci P. v nemocnici sú rozdelení na skoré (1-6 dní po operácii) a neskoro (od 6. dňa pred prepustením z nemocnice). Počas P. P. z p. Sa rozlišujú štyri fázy: katabolický, reverzný vývoj, anabolický a fázový prírastok hmotnosti. Prvá fáza je charakterizovaná zvýšeným vylučovaním dusíkatých odpadov močom, dysproteinémiou, miernou hypovolémiou a stratou telesnej hmotnosti. Pokrýva skoré a čiastočne neskoré pooperačné obdobie. Vo fáze reverzného vývoja a anabolickej fázy, pod vplyvom hypersekrécie anabolických hormónov (inzulín, somatotrop, atď.), Prevláda syntéza: obnovuje sa metabolizmus elektrolytov, proteínov, sacharidov a tukov. Potom začína fáza zvýšenia telesnej hmotnosti, ktorá spravidla spadá do obdobia, keď je pacient v ambulantnej liečbe.
Hlavnými bodmi pooperačnej intenzívnej starostlivosti sú: primeraná úľava od bolesti, udržiavanie alebo korekcia výmeny plynov, zabezpečenie adekvátneho prekrvenia, korekcia metabolických porúch, ako aj prevencia a liečba pooperačných komplikácií. Pooperačná analgézia sa dosahuje podávaním narkotických a narkotických analgetík s použitím rôznych typov anestézie. Pacient by nemal cítiť bolesť, ale liečebný program by mal byť navrhnutý tak, aby anestézia neznižovala vedomie a dýchanie.
Po prijatí pacienta po operácii na jednotku intenzívnej starostlivosti a intenzívnej starostlivosti je potrebné určiť dýchacie cesty, frekvenciu, hĺbku a rytmus dýchania, farbu kože. Porušenie dýchacích ciest u oslabených pacientov v dôsledku stázy jazyka, akumulácie v dýchacích cestách krvi, spúta, obsahu žalúdka si vyžadujú terapeutické opatrenia, ktorých povaha závisí od príčiny porušenia priechodnosti. Medzi tieto opatrenia patrí maximálne predĺženie hlavy a odstránenie dolnej čeľuste, vloženie vzduchového potrubia, odsávanie kvapalného obsahu z dýchacích ciest, bronchoskopická rehabilitácia tracheobronchiálneho stromu. Ak sa objavia príznaky závažného respiračného zlyhania, pacient má byť intubovaný a prenesený mechanické vetranie .
Poruchy centrálnych mechanizmov respiračnej regulácie, ktoré sú spravidla výsledkom depresie respiračného centra pod vplyvom anestetík a omamných látok používaných počas operácie, môžu viesť k akútnym respiračným poruchám. Základom intenzívnej liečby akútnych respiračných porúch centrálnej genézy je umelé dýchanie (ALV), ktorého metódy a možnosti závisia od povahy a závažnosti respiračných porúch.
Porušenie periférnych mechanizmov regulácie respirácie, často spojené so zvyškovou relaxáciou svalov alebo recuráciou, môže viesť k zriedkavému narušeniu výmeny plynov a zástavy srdca. Okrem toho sú tieto poruchy možné u pacientov s myasténiou, u iných pacientov Intenzívna liečba porúch periférneho dýchania spočíva v udržiavaní výmeny plynov ventilaciou masky alebo opakovanej intubácii priedušnice a pri prechode na mechanickú ventiláciu až do úplného obnovenia svalového tonusu a adekvátneho nezávislého dýchania.
Ťažké respiračné ochorenia môžu byť spôsobené pľúcnou atelektázou, pľúcnou embólií pneumóniou. S výskytom klinických príznakov atelektázy a rádiologického potvrdenia diagnózy je potrebné odstrániť predovšetkým príčinu atelektázy. Pri atelektáze kompresie sa to dosiahne vypustením pleurálnej dutiny a vytvorením vákua. Keď obštrukčná atelektáza vykonáva terapeutickú bronchoskopiu s rehabilitáciou tracheobronchiálneho stromu. V prípade potreby sa pacient prenesie do ventilátora. Komplex terapeutických opatrení zahŕňa použitie aerosólových foriem bronchodilatátorov, perkusiu a vibračnú masáž hrudníka, posturálnu drenáž.
Výskyt dyspnoe je vždy alarmujúcim príznakom, najmä v 3. až 6. deň pct Príčiny dyspnoe v pcte môžu byť septika, pleura, pľúcny edém atď. Náhla nemotivovaná dyspnoe charakteristická pre tromboembolizmus pľúcnej artérie by mala upozorniť lekára ,
Cyanóza, bledosť, mramorovaná farba pleti, fialové, modré škvrny sú príznakmi pooperačných komplikácií. Vzhľad žltej kože a skléry často poukazuje na závažné hnisavé komplikácie a rozvoj zlyhania pečene. Oligoanúria a anúria indikujú najzávažnejšiu pooperačnú situáciu - zlyhanie obličiek.
Pokles hemoglobínu a hematokritu je dôsledkom nedokončenej operačnej straty krvi alebo pooperačného krvácania. Pomalý pokles hemoglobínu a počet erytrocytov indikujú potlačenie erytropoézy toxického genézu. Pre zápalové komplikácie je charakteristická hyperleukocytóza, lymfopénia alebo recidíva po normalizácii krvného vzorca. Mnohé biochemické parametre krvi môžu indikovať operatívne komplikácie. Zvýšenie hladiny amylázy v krvi a moči sa teda pozoruje počas pooperačnej f (ale je to možné aj pri parotitíde, ako aj pri obštrukcii črevného traktu); transaminázy - s exacerbáciou a, infarktu myokardu, pečene; krvný bilirubin - s e, obštrukčnou žltačkou, pylephlebitídou; močoviny a kreatinínu v krvi - s rozvojom akútneho zlyhania obličiek.
Hlavné komplikácie pooperačného obdobia , Preháňanie chirurgickej rany je najčastejšie spôsobené aeróbnou flórou, ale často je pôvodcom anaeróbna neklostridiálna mikroflóra. Komplikácie sa zvyčajne prejavujú na 5. - 8. deň Pct, ktorý sa môže vyskytnúť aj po prepustení z nemocnice, ale rýchly rozvoj hnisania je možný aj v 2. - 3. deň. Pri hnisaní rany sa telesná teplota spravidla znovu zvyšuje a má zvyčajne febrilnú povahu. Mierna, s anaeróbnou neklostridiálnou flórou - značená lymfopénia, toxická granularita neutrofilov. Diuréza sa spravidla neporušuje.
Lokálne príznaky hnisania rany sú opuch v oblasti stehov, návaly horúčavy, ostré bolesti pri pohmate. Ak je však hnisanie lokalizované pod aponeurózou a nerozšíri sa do podkožného tkaniva, tieto príznaky, s výnimkou bolesti pri hmatovom vyšetrení, nemusia byť prítomné. U pacientov s pokročilým a starým vekom sa často vymažú všeobecné a lokálne príznaky hnisania a prevalencia procesu však môže byť veľká.
Liečba spočíva v nariedení okrajov rany, jej dezinfekcii a odkvapkaní a obväzovaní antiseptikami. Pri výskyte granulácií predpíšte obväzy na masti, naneste sekundárne švy. Po starostlivej excízii hnisavých-nekrotických tkanív sú možné šitie cez drenáž a ďalšie premývanie rany ranou rôznymi antiseptikami s konštantným aktívnym odsávaním.